COMMUNIQUE DE PRESSE
Genzyme annonce les résultats positifs d’une étude de Phase 3 avec Alemtuzumab (LEMTRADATM*) dans la sclérose en plaques
– Efficacité significative d’alemtuzumab par rapport à l’interféron bêta-1a (Rebif®) observée sur les deux critères principaux d’évaluation, les rechutes et le handicap, chez les patients atteints de Sclérose en Plaques déjà traités auparavant –
– Genzyme confirme l’objectif de soumission du dossier au premier trimestre 2012 –
Paris, France – Le 14 novembre 2011 – Sanofi (EURONEXT: SAN et NYSE: SNY) et sa filiale
Genzyme annoncent aujourd’hui que l’étude de Phase 3 CARE-MS II a atteint ses deux critères principaux combinés d’évaluation. Le taux de rechutes et l’accumulation (ou aggravation) soutenue du handicap ont été réduits de manière significative chez les patients atteints de sclérose en plaques ayant reçu alemtuzumab (LEMTRADATM) comparativement à Rebif® (44 mcg d’interféron bêta-1a par voie sous-cutanée). Les résultats obtenus au titre de ces deux critères combinés principaux d’évaluation sont statistiquement très significatifs. CARE-MS II est l’étude randomisée de Phase 3 comparant l’agent expérimental alemtuzumab à l’interféron bêta-1a chez des patients atteints de sclérose en plaques (SEP) de type récurrente-rémittente. Les patients devaient avoir subi une rechute lorsqu’ils étaient sous un traitement précédent afin de pouvoir être inclus dans l’étude CARE-MS II.
Genzyme développe alemtuzumab dans la sclérose en plaques en collaboration avec Bayer
HealthCare.
Dans cette étude randomisée qui a inclus 840 patients, une réduction de 49 pour cent du taux de rechute a été observée chez les patients traités par alemtuzumab 12 mg en comparaison avec l’interféron bêta-1a au cours des deux ans de l’étude (p<0,0001). Il est important de noter qu'il y a eu
également une réduction de 42 pour cent du risque d'accumulation (ou aggravation) soutenue du handicap, mesurée par le score sur l'échelle EDSS (Expended Disability Status Scale), (p=0,0084).
L'analyse des données complètes de l'étude CARE-MS II est en cours et les résultats seront présentés dans le cadre d'un prochain congrès scientifique.
« CARE-MS ll représente le point culminant de nombreuses années de recherche clinique et en laboratoire visant à démontrer le potentiel d'alemtuzumab comme traitement très efficace dans la sclérose en plaques et à comprendre les mécanismes liés à l'histoire complexe de la maladie, " a déclaré le professeur Alastair Compston, Président du Comité de pilotage chargé de la conduite de l'étude et Directeur du Département de neurosciences cliniques à l'Université de Cambridge au
Royaume-Uni. « Pris dans leur ensemble, les données des essais de Phase 2 et 3 montrent qu'alemtuzumab a la possibilité de devenir un traitement qui transforme la vie des personnes atteintes de sclérose en plaques récurrente. »
L'étude CARE-MS II a comparé le traitement avec alemtuzumab 12 mg donné quotidiennement par voie intraveineuse pendant 5 jours puis de nouveau pendant 3 jours un an plus tard, au traitement avec 44 mcg d'interféron bêta-1a administré par injection sous-cutanée trois fois par semaine pendant les deux ans de l'étude.
« Les résultats supérieurs d'efficacité pour alemtuzumab, en particulier le ralentissement du handicap, sont très encourageants car il s'agissait d'une étude comparative directe avec la forte dose d'interféron bêta-1a par voie sous-cutanée » a déclaré le Docteur Jeffrey Cohen, Professeur de
Médecine (Neurologie) au Lerner College de la Cleveland Clinic; Directeur de Thérapie Expérimentale 1/4
La présente information ne constitue qu’un extrait du communiqué ci-après : Télécharger le communiqué complet
!:!iframe http://www.nextnews.fr/upload/fr/nextnews%5Fsanofi%5Fgenzyme%5Fannonce%5Fles%5Fresultats%5Fpositifs%5Fd%92une%5Fetude%5Fde%5Fphase%5F3%5Favec%5Falemtuzumab%5Flemtradatm%5Fdans%5Fla%5Fsclerose%5Fen%5Fplaques%5F57226%2EPDF!:!
En partenariat avec NextNews
En aucun cas la résponsabilité du site lemediascope.fr ne pourra être engagée en cas d’éventuelle réclamation.
| Partager : |
|
Tweet |
|
|
|
| ||||


 Chaînes INFO : part d’audience dimanche 15 octobre 2023-
Chaînes INFO : part d’audience dimanche 15 octobre 2023- (Vidéo) Rugby : France – Afrique du Sud : l’arbitrage pas » au niveau » ( Antoine Dupont) : « Je ne suis pas sûr que l’arbitrage ait été au niveau »
(Vidéo) Rugby : France – Afrique du Sud : l’arbitrage pas » au niveau » ( Antoine Dupont) : « Je ne suis pas sûr que l’arbitrage ait été au niveau » TF1 audience France /Afrique du Sud (Coupe du Monde Rugby) + 20h30 le dimanche ( Mick Jagger) + TF1 / France 2 ( 20h) + » Beau Geste » ( F2)
TF1 audience France /Afrique du Sud (Coupe du Monde Rugby) + 20h30 le dimanche ( Mick Jagger) + TF1 / France 2 ( 20h) + » Beau Geste » ( F2) TF1 audience « 50 minutes Inside » (Isabelle Ithurburu) / C l’Hebdo (Aurelie Casse) / « N’Oubliez pas les paroles » ( F2) / M6 le journal 19h45
TF1 audience « 50 minutes Inside » (Isabelle Ithurburu) / C l’Hebdo (Aurelie Casse) / « N’Oubliez pas les paroles » ( F2) / M6 le journal 19h45 TF1 Audience rugby Irlande/ Nouvelle Zélande All Blacks ( 24/28) ( Coupe du monde)/ 20h30 le Samedi (Delahousse) / Bernadette Chirac / Catherine Deneuve, icône pop) + 20h (TF1- FRANCE 2)
TF1 Audience rugby Irlande/ Nouvelle Zélande All Blacks ( 24/28) ( Coupe du monde)/ 20h30 le Samedi (Delahousse) / Bernadette Chirac / Catherine Deneuve, icône pop) + 20h (TF1- FRANCE 2) ( Vidéo) la Russie accusée de soutenir le Hamas face à Israël
( Vidéo) la Russie accusée de soutenir le Hamas face à Israël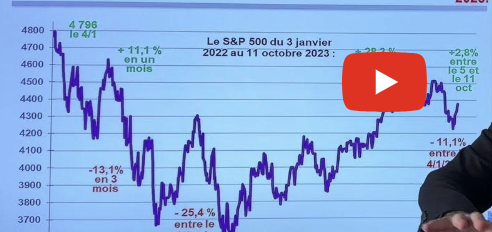 (Vidéo) Economie 2024 : Pourquoi ça ne va pas s’arranger ? ( l’économiste Marc Touati)
(Vidéo) Economie 2024 : Pourquoi ça ne va pas s’arranger ? ( l’économiste Marc Touati) Arras: enseignant égorgé / 2 blessés graves- le suspect Fiché S contrôlé la veille / Macron annonce « un autre attentat déjoué dans une autre région »
Arras: enseignant égorgé / 2 blessés graves- le suspect Fiché S contrôlé la veille / Macron annonce « un autre attentat déjoué dans une autre région » Israël contre attaque imminente contre le Hamas qui détient les otages : l’évacuation d’1 million d’habitants du nord de la bande de Gaza ordonnée sous 24h
Israël contre attaque imminente contre le Hamas qui détient les otages : l’évacuation d’1 million d’habitants du nord de la bande de Gaza ordonnée sous 24h